Adjuvant behandling i monoterapi
Bivirkninger i KEYNOTE-5645
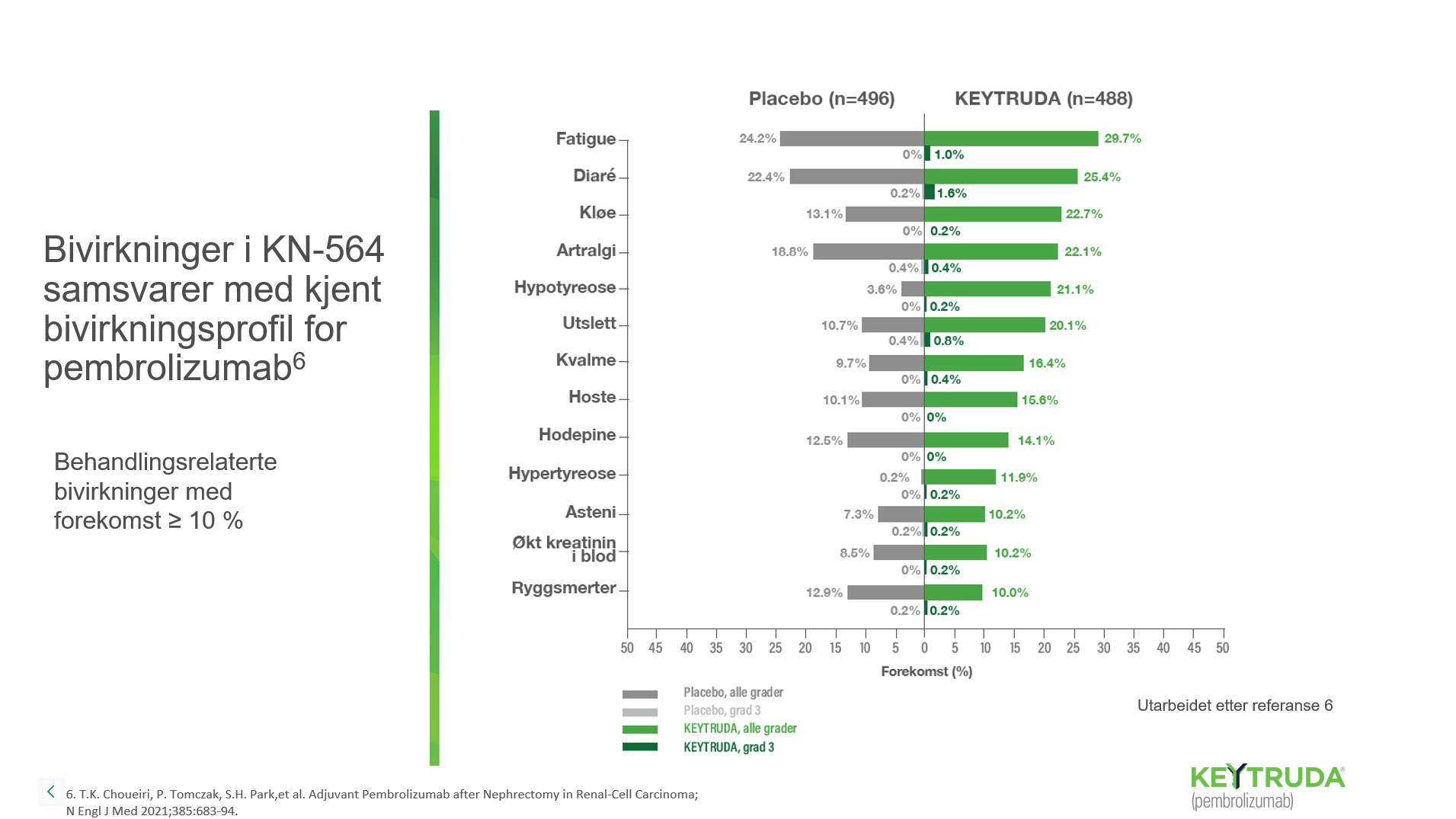
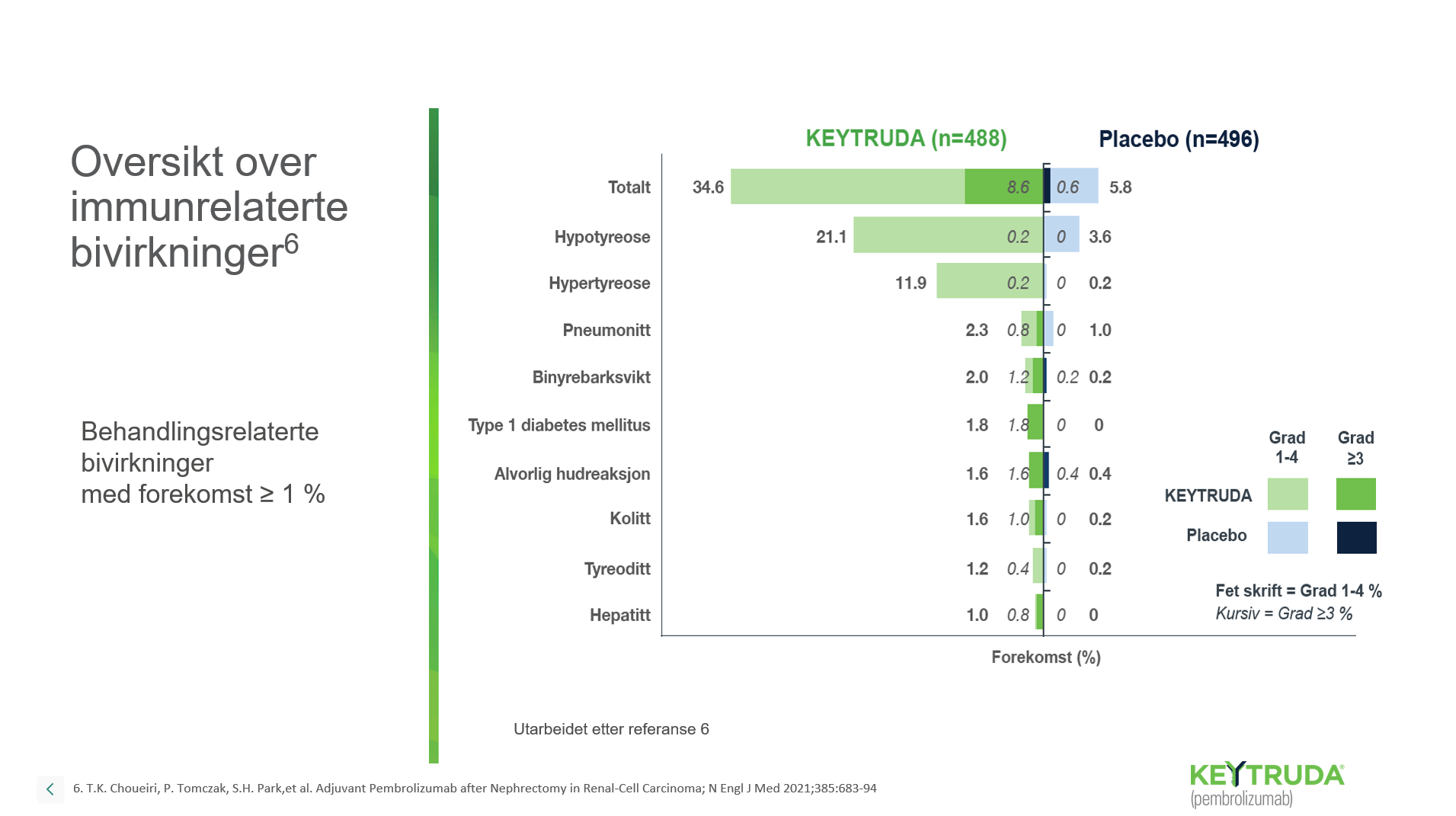
Oppsummering av sikkerhetsprofilen til KEYTRUDA®1
Pembrolizumab (KEYTRUDA®) er vanligst assosiert med immunrelaterte bivirkninger. De fleste immunrelaterte bivirkninger som forekom under behandling med KEYTRUDA® var reversible og ble håndtert ved seponering av KEYTRUDA®, administrering av kortikosteroider og/eller støttende behandling1.
Se utfyllende informasjon i preparatomtalen, i utvalgt sikkerhetsinformasjon og bivirkninger.
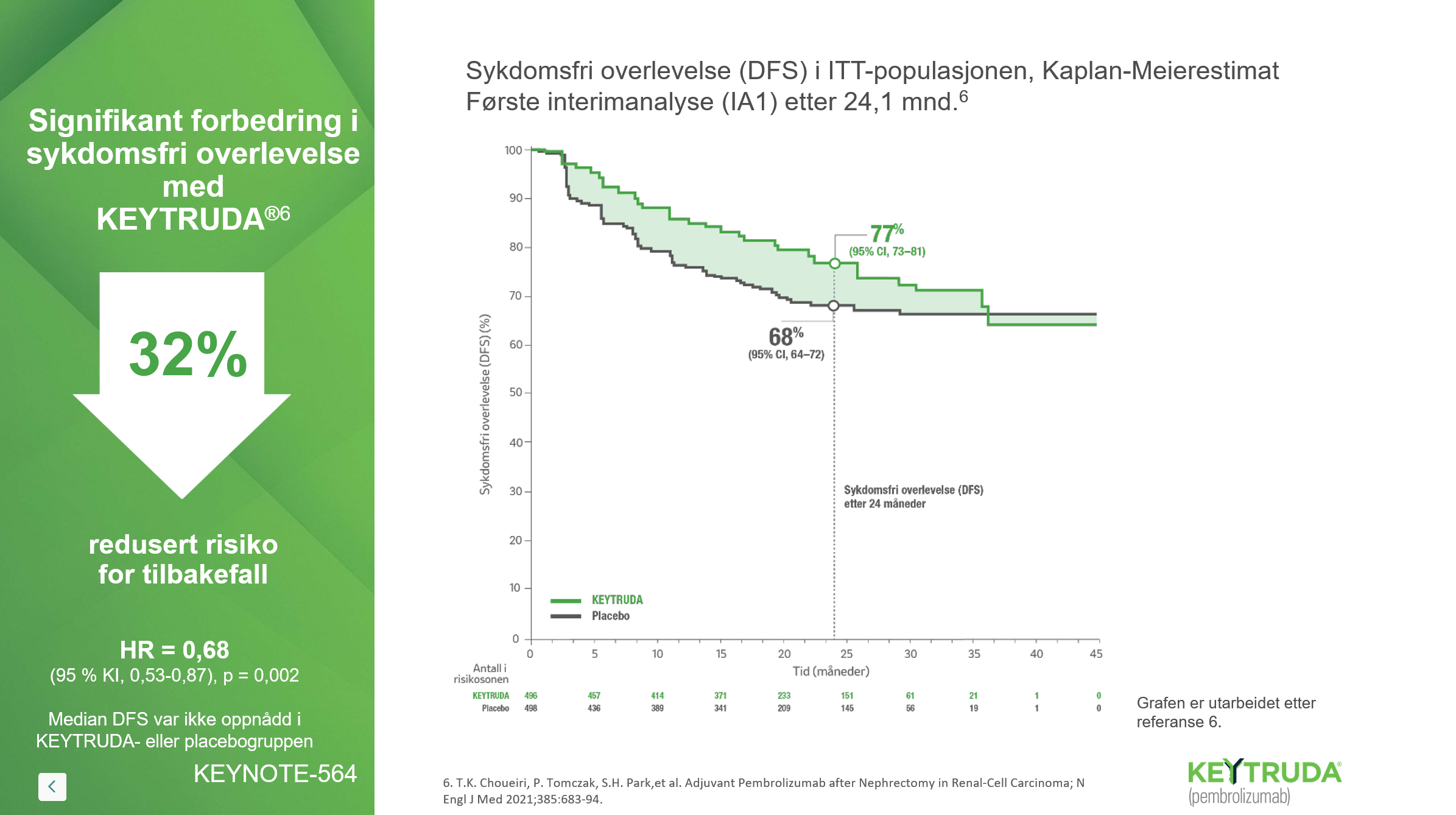
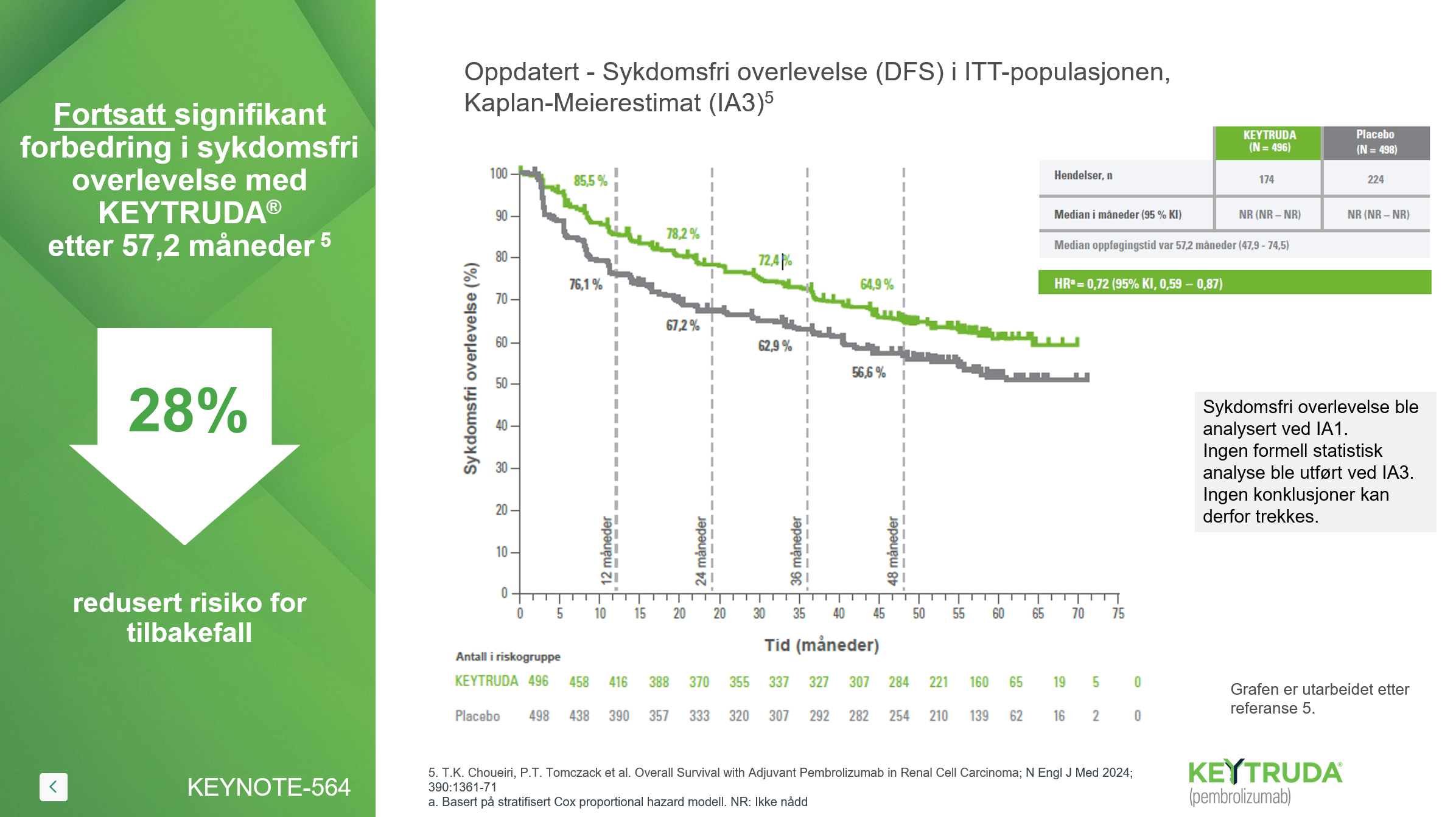
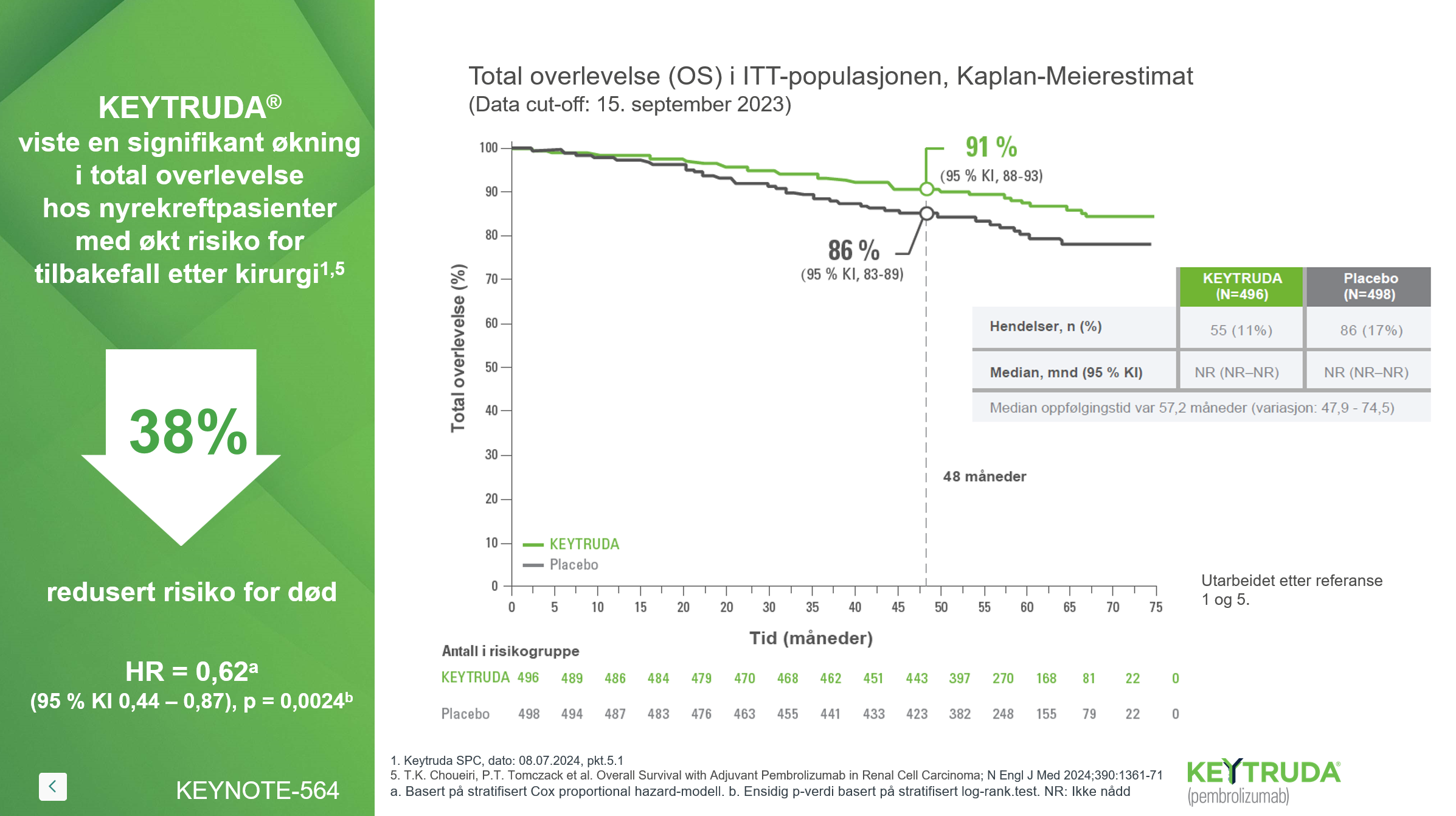
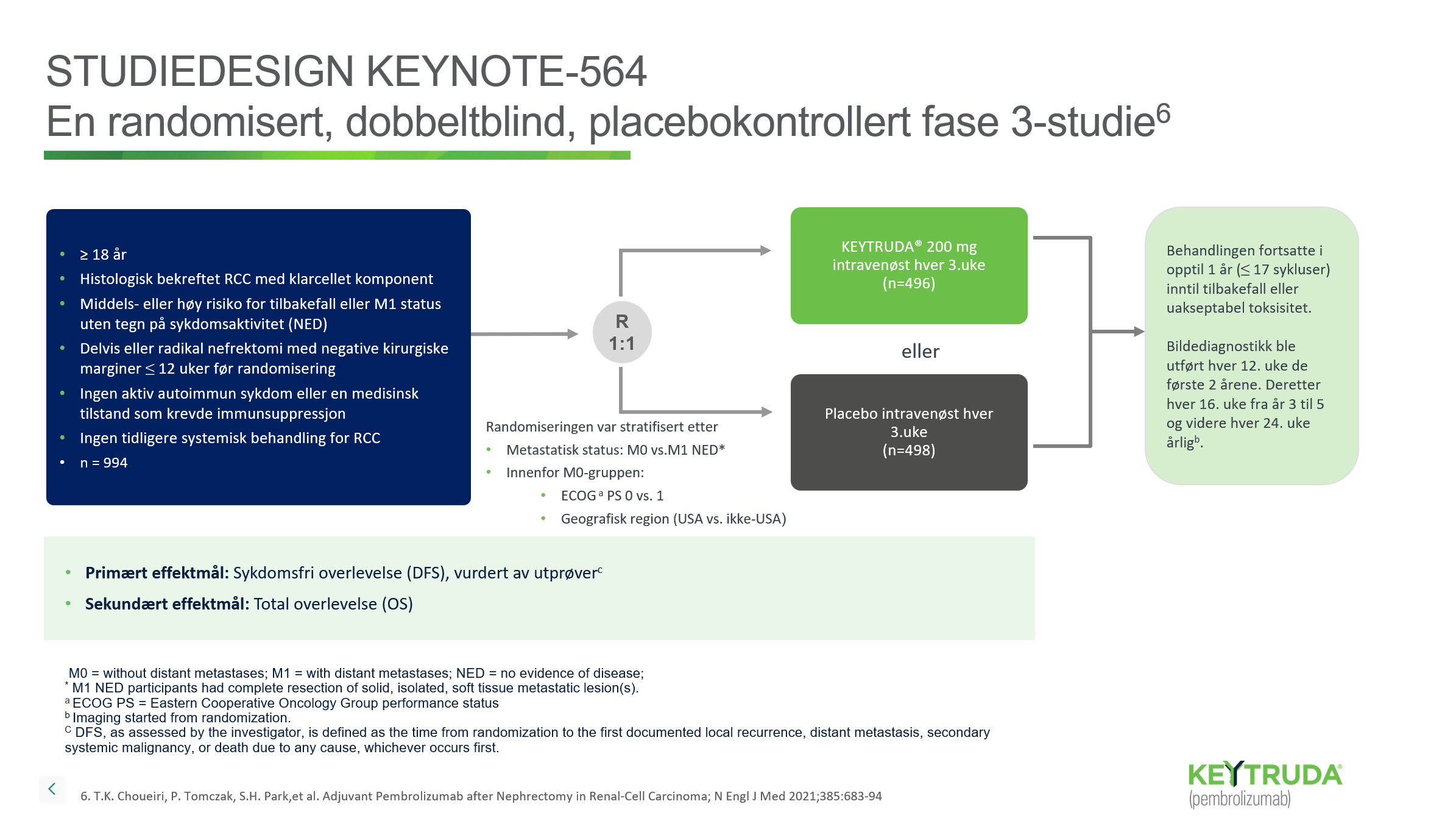
Studiedesign KEYNOTE-5645
KEYNOTE-564 er en randomisert, dobbeltblind, placebo-kontrollert fase 3-studie som undersøker adjuvant behandling av nyrecellekarsinom.
Studien inkluderer 994 pasienter med middels eller høy risiko for tilbakefall etter nefrektomi.
Dosering1
Ved adjuvant behandling av nyrecellekarsinom skal KEYTRUDA® gis inntil tilbakefall, uakseptabel toksisitet eller i en periode på opptil 1 år.
KEYTRUDA kan gis hver 3. eller 6.uke. Les mer om dosering her: Keytruda – Dosering | MSD Innsikt

Nå er nasjonalt handlingsprogram for nyrekreft oppdatert
Revidert 27. september 2024
Har du spørsmål rundt KEYTRUDA®?
Ta kontakt med meg.

Vedrana Grcic-van de Pavert – Brand & Customer Manager

Bente Arvesen – Key Account Manager Oncology
Referanser
- Keytruda SPC, August 2024, 4.1, 4.2, 4.8, 5.1
- Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølging av pasienter med nyrekreft [nettdokument]. Oslo: Helsedirektoratet (siste faglige endring 27. september 2024). Tilgjengelig fra https://www.helsedirektoratet.no/retningslinjer/nyrecellekreft-handlingsprogram
- Sundaram M, et al. Clinical and economic burdens of recurrence following nephrectomy for intermediate high- or high-risk renal cell carcinoma: A retrospective analysis of Surveillance, Epidemiology, and End Results–Medicare dataJ Manag Care Spec Pharm. 2022;28(10):1149-1160, with supplement
- Bencina G, Billeskov R, Bak R, Al-Sabbagh A, Pedersen JH, Lunetcas M, et al. Recurrence patterns following nephrectomy for renal cell carcinoma in a Danish nationwide cohort. Bjui Compass. 2024, 1-8
- T.K. Choueiri, P. Tomczak, S.H. Park,et al. Adjuvant Pembrolizumab after Nephrectomy in Renal-Cell Carcinoma; N Engl J Med 2021;385:683-94
- T.K. Choueiri, P.T. Tomczack et al. Overall Survival with Adjuvant Pembrolizumab in Renal-Cell Carcinoma; N Engl J Med 2024;390:1361-71
- Powles T, Albiges L, Bex A, et al.. Renal cell carcinoma: Esmo Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol. 2024;35(8):692-706
- Bedke J, Albiges L, Capitanio U, et al. 2021 Updated European Association of Urology Guidelines on the Use of Adjuvant Pembrolizumab for Renal Cell Carcinoma. European urology. 2022;81(2):134-7
- https://www.nyemetoder.no/metoder/pembrolizumab-keytruda-indikasjon-xx/